
服务热线

脑缺血后乳酸大量积聚,作为中枢神经系统的能量来源,乳酸在能量危机期间,可以缓解神经元中的能量缺乏。此外,乳酸还具有调节神经元功能的基本信号传导作用,包括兴奋性、可塑性和记忆巩固。然而乳酸调节这些代谢和细胞功能的机制尚未完全阐明。
南京大学医学院附属鼓楼医院徐运、陈燕婷团队在Advanced Science上发表题为“MeCP2 Lactylation Protects against Ischemic Brain Injury by Transcriptionally Regulating Neuronal Apoptosis”的研究论文,探讨了赖氨酸乳酸化(一种乳酸的表观遗传修饰)在脑缺血中的作用。使用小鼠短暂性大脑中动脉闭塞(MCAO)模型,观察到脑乳酸水平升高和整体蛋白质乳酸化,系统探讨了非组蛋白乳酸化对缺血后神经元命运的调控机制。

蛋白乳酸化在缺血卒中中呈神经保护作用
大脑中动脉闭塞(MCAO)模型后1天,小鼠脑组织缺血脑半球乳酸水平达到峰值(图1A)。使用糖酵解抑制剂(2-脱氧葡萄糖2-DG)或乳酸转运抑制剂(4-羟基肉桂酸4-CIN)后,加重了梗死及神经功能缺损(图1E-G);而给予乳酸钠后梗死体积显著缩小,且神经功能得到改善(图1M-P)。提示蛋白质乳酸化对缺血性脑损伤具有保护作用。研究发现卒中后大脑中泛乳酸化主要在神经元中显著诱导,表明蛋白质乳酸化在缺血性损伤后主要定位于神经元。
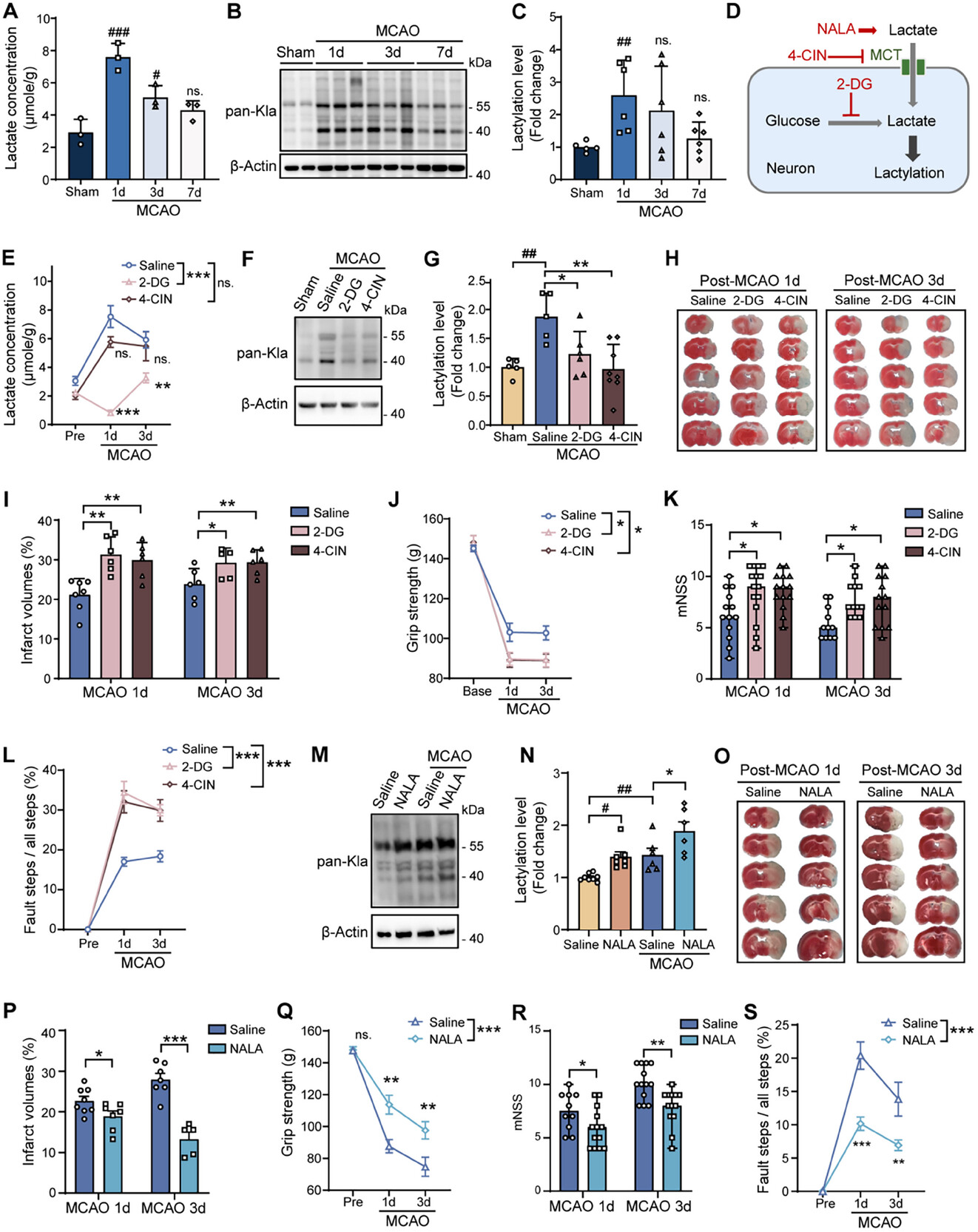
图1 蛋白质乳酸化及其在缺血性卒中中的神经保护作用
脑缺血诱导蛋白质乳酸化组学重塑
为了鉴定并量化受脑缺血显著影响的脑蛋白中乳酸化修饰,研究对MCAO小鼠和对照小鼠的半影区进行分析。鉴定到468种蛋白的1402个乳酸化修饰位点,其中68种蛋白的97个位点上调(图2G)。MCAO小鼠中MeCP2乳酸化上调,在缺血皮质中表达稳定且主要定位于细胞核,其多个乳酸化位点参与急性脑缺血中的包括“神经元死亡”在内的几个顶部富集的生物过程(图2I)。因此推测MeCP2的乳酸化修饰可能在调节急性缺血性卒中神经元死亡中起作用。而2-DG或4-CIN处理后MeCP2乳酸化显著降低。
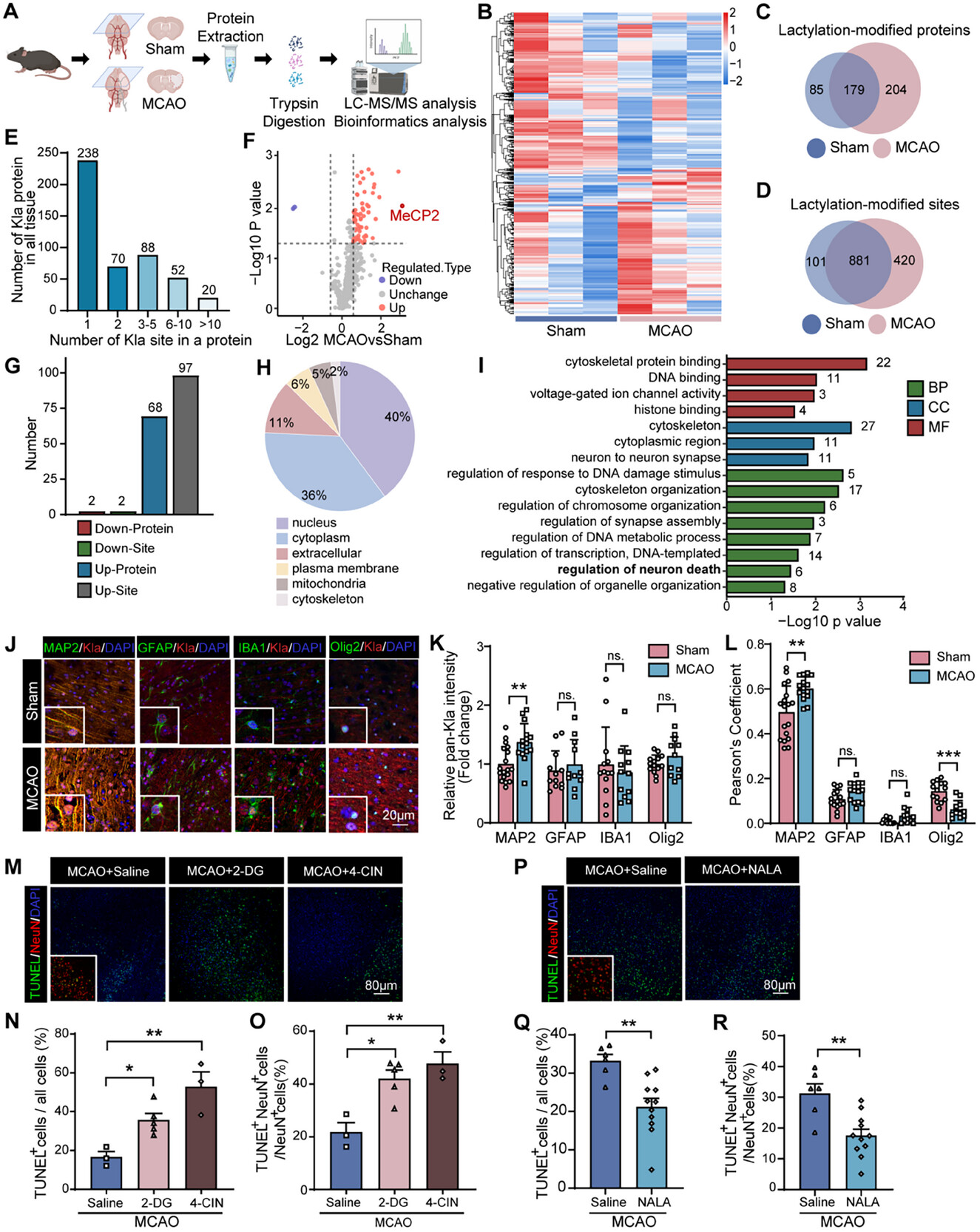
图2 蛋白质乳酸化可保护中风后神经元免于凋亡
乳酸化水平决定缺血后神经元凋亡程度
为确认不同乳酸化修饰水平对MCAO后神经元死亡的影响,研究进行了流式细胞术分析。数据显示,接受2-DG或4-CIN治疗的MCAO小鼠神经元死亡比例显著增加,而接受NALA后神经元死亡比例减少。这表明,乳酸化修饰在神经元存活中的潜在保护作用,其减少与MCAO术后神经元死亡增加相关。
同时,蛋白质免疫印迹(Western blot)分析显示,在MCAO术后1天和3天,焦亡标志物裂解的caspase-1水平未升高,而作为坏死性凋亡标志物的磷酸化RIP3(p-RIP3)显著上调。针对乳酸化修饰的干预措施对p-RIP3水平无显著影响。表明蛋白质乳酸化选择性调控凋亡通路,在应对缺血性损伤时,乳酸化修饰主要影响神经元凋亡,而非焦死或坏死性凋亡。
蛋白质乳酸化可减轻缺氧-复氧处理后神经元凋亡
为深入探究乳酸化在缺血条件下调节神经元死亡通路的作用,研究建立了缺氧-复氧(OGD/R)模型。分析评估复氧后不同时间点的裂解型caspase-3水平来反映细胞凋亡状态。结果显示,复氧6小时后裂解型caspase-3表达量较对照组显著升高。在探究乳酸化阻断对缺血条件下细胞存活率及凋亡的影响的实验中,提示2-DG处理导致细胞活力呈剂量依赖性下降,在4 mM及更高浓度时观察到显著降低,且4 mM浓度的2-DG在缺氧/再灌注(OGD/R)条件下显著降低蛋白质乳糖化水平,并伴随裂解型caspase-3的显著诱导。相反,NALA处理显著上调泛蛋白质乳酸化水平,减轻OGD/R后神经元凋亡。表明乳酸化在维持细胞存活中具有保护作用。2-DG诱导的低乳酸化水平加剧细胞凋亡,而NALA等增强乳酸化的处理通过减少细胞死亡和促进细胞存活发挥神经保护作用。
MeCP2为缺血诱导乳酸化的关键非组蛋白
为验证MCAO小鼠中候选蛋白质乳酸化修饰标志物,研究采用平行反应监测(PRM)技术对潜在乳酸化修饰蛋白进行定量分析。结果显示,MeCP2蛋白K210位点、Npm1蛋白K221位点及Snca蛋白K96位点的乳酸化修饰水平在MCAO小鼠中显著上调(图3B)。
为进一步探究MeCP2在缺血性损伤响应中的作用,研究分析了其在MCAO小鼠缺血皮层中的时间表达模式。结果显示,脑缺血后早期阶段MeCP2表达水平保持相对稳定。在MCAO术后24小时小鼠半暗带区域的MeCP2蛋白上鉴定,卒中显著诱导MeCP2蛋白K210和K249位点的乳酸化修饰,并参与急性脑缺血中多个显著富集的生物学过程。因此推测MeCP2蛋白的乳酸化修饰可能在急性缺血性脑卒中神经元死亡的调控中发挥作用。
免疫共沉淀(Co-IP)实验显示,MCAO小鼠中MeCP2的乳酸化修饰水平上调,而2-DG或4-CIN治疗可显著降低该修饰水平(图3C)。通过NeuN标记的皮质切片免疫荧光染色及邻位连接技术(PLA)分析证实,MeCP2的乳酸化修饰与神经元细胞共定位,表明该修饰主要发生于神经元中(图3D)。
MeCP2的乳酸化修饰通过转录调控神经元死亡
进一步研究显示,MCAO组中MeCP2等关键转录相关蛋白的乳酸化修饰水平发生显著变化,表明MeCP2在缺血条件下可作为转录调控因子发挥作用(图3E)。MeCP2结合峰主要富集于转录起始位点(TSS),主要定位于启动子区域(图3F、G)。进一步分析与凋亡通路相关的差异结合峰,发现MCAO术后MeCP2在Pdcd4和Pla2g6基因启动子区域的结合增加,该结合可被2-DG/4-CIN减弱(图3I)。
荧光素酶报告基因实验显示,MeCP2过表达显著降低了Pdcd4/Pla2g6启动子活性(图3J、K),表明MeCP2可结合至凋亡通路相关基因的启动子区域,发挥转录抑制作用。染色质免疫沉淀定量聚合酶链式反应(ChIP-qPCR)进一步证实MeCP2乳酸化增强其与靶启动子的结合并抑制基因表达。此外,定量聚合酶链式反应(qPCR)分析进一步证实了乳酸化修饰对下游基因表达的影响。这些观察结果表明,MeCP2的乳酸化修饰增强了其与靶基因启动子区域的结合亲和力,并从转录水平抑制了参与神经元凋亡相关基因的表达。
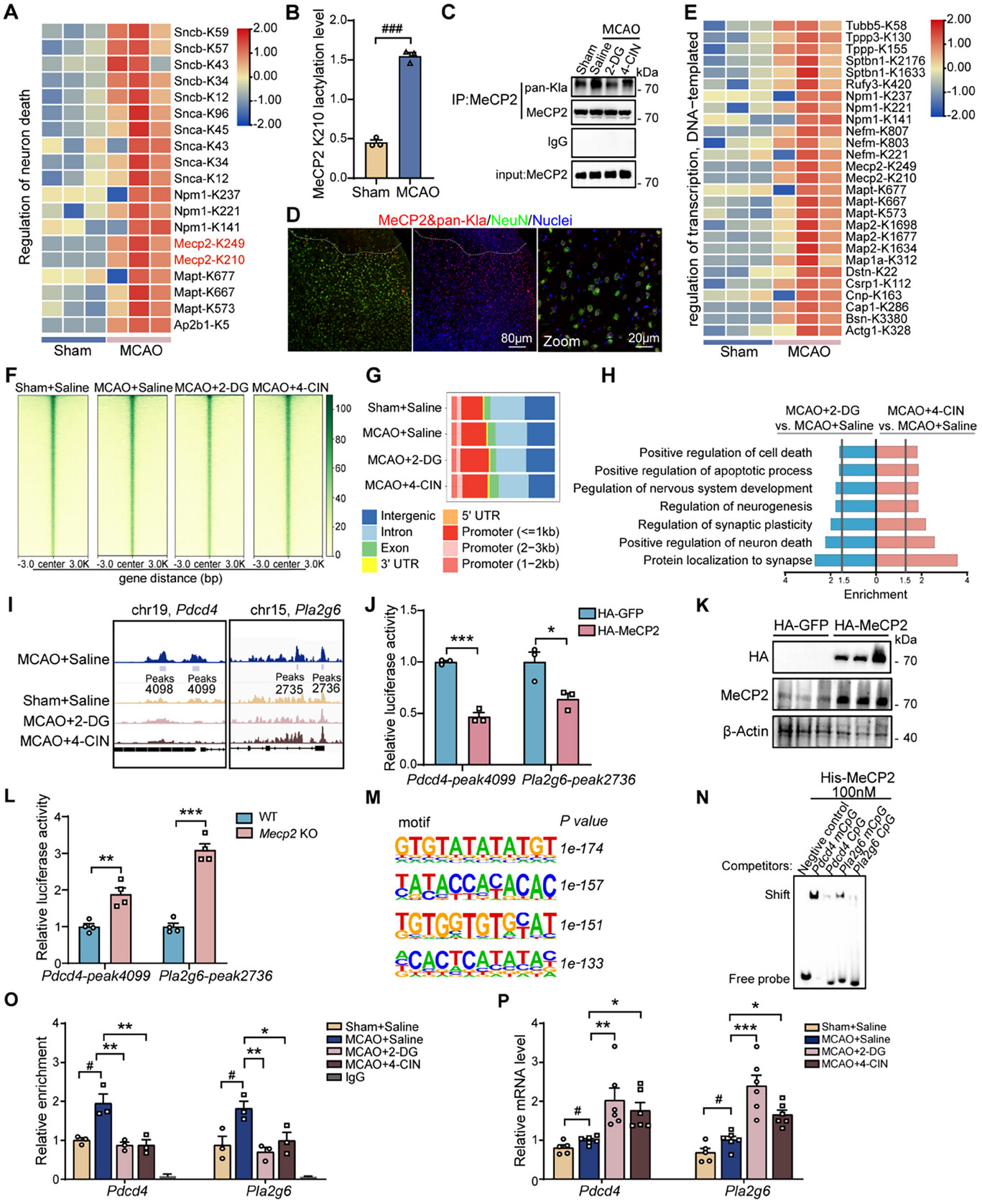
图3 MeCP2乳酸化调节卒中后神经元凋亡
PDCD4与GVIA PLA2参与缺血后神经元凋亡
为探究PDCD4和GVI PLA2在缺血性脑卒中中的作用,研究对MCAO术后1天、3天及7天收集的皮层组织进行了蛋白质免疫印迹分析。结果显示表明神经元中PDCD4的表达在缺血应激7天迅速上调。而GVI PLA2的表达在卒中后随时间推移逐渐增加。在GVI PLA2过表达对神经元凋亡的影响的研究中显示,GVI PLA2过表达(OE)导致裂解的caspase-3水平升高,表明细胞凋亡增强。此外,在氧糖剥夺/复氧(OGD/R)条件下,使用GVI PLA2特异性抑制剂BEL治疗可显著降低GVI PLA2和内质网应激标志物CHOP的表达水平。这表明,缺血性脑卒中后PDCD4和GVI PLA2的表达均上调,且GVI PLA2在缺血条件下可加剧神经元凋亡和内质网应激。
MeCP2在K210和K249位点的乳酸化修饰通过转录抑制作用抑制Pdcd4和Pla2g6基因表达
在Mecp2基因敲除的HEK293T细胞中表达了HA标记的全长或截短型MeCP2蛋白,发现MeCP2的乳酸化修饰主要发生在转录抑制结构域(TRD)。通过分析多物种间MeCP2的TRD结构域序列比对,鉴定出保守的乳酸化修饰位点及其周围区域(图4A)。免疫共沉淀实验表明,K210或K249位点的突变显著降低了MeCP2的乳酸化修饰水平(图4B),荧光素酶报告基因实验显示,K210R和K249R MeCP2突变导致Pdcd4和Pla2g6的转录水平显著升高(图4C、D)。MeCP2的双位点突变(K210R/K249R)显著削弱了其乳酸化修饰水平及其对Pdcd4和Pla2g6的转录抑制作用(图4E-G)。此外,重组MeCP2蛋白与Pdcd4和Pla2g6基因启动子区域结合能力较强,而K210R/K249R突变体的结合亲和力显著降低(图4H),表明乳酸化修饰在增强MeCP2与DNA结合能力中的作用。
此外,研究发现MeCP2的K210R/K249R位点突变会增强神经元细胞在OGD条件下的凋亡倾向(图4I、J)。在OGD条件下,表达MeCP2 K210R/K249R双突变体的神经元中GVI PLA2和PDCD4的蛋白水平均上调(图4K-M)。这些表明,MeCP2在K210和K249位点的乳酸化修饰增强了其结合至Pdcd4和Pla2g6基因启动子区富含甲基化CpG区域的能力,从而调控这些基因的表达,并保护神经元免受缺血诱导的细胞凋亡。
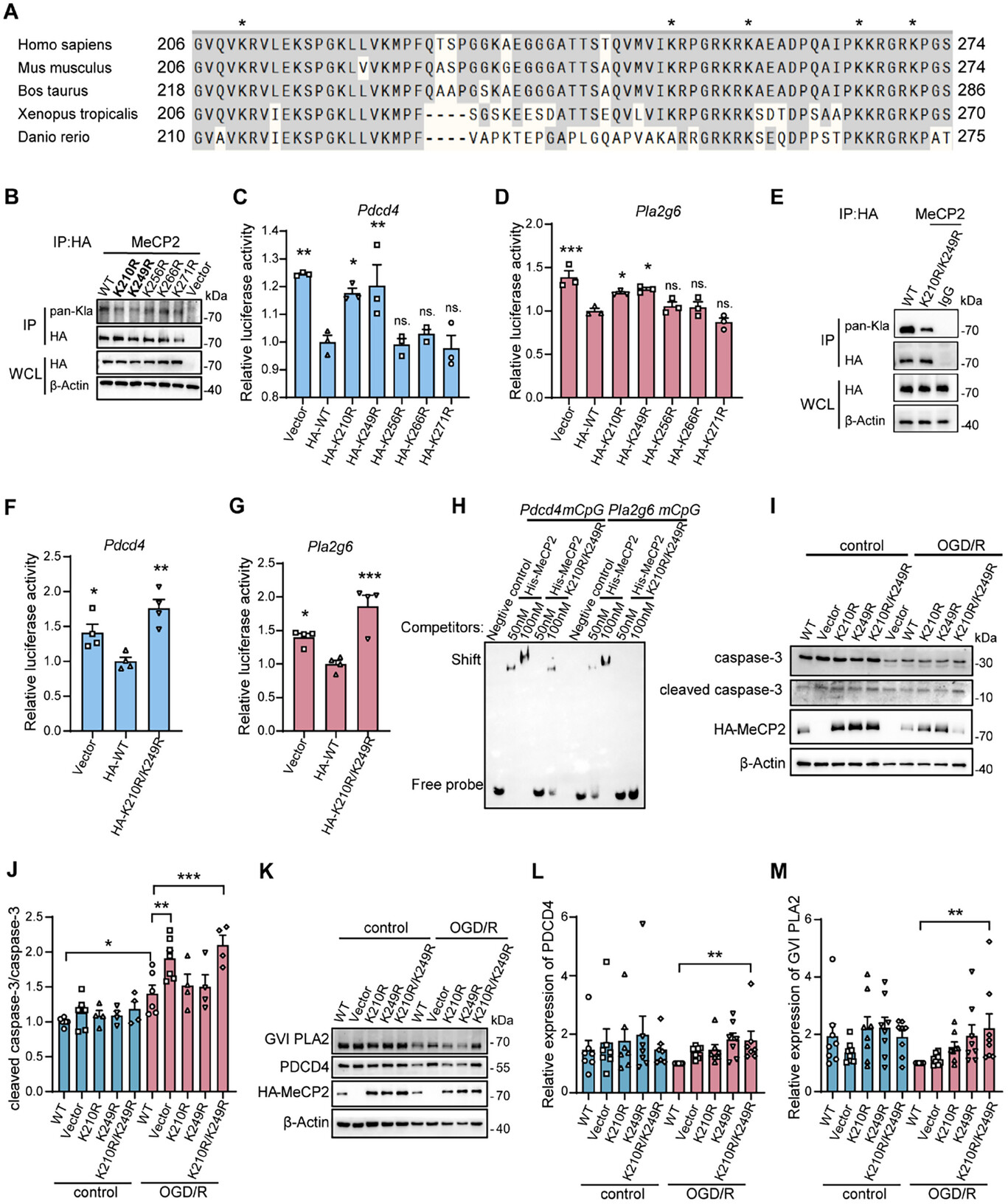
图4 MeCP2在K210和K249位点的乳糖醛酸化调节中风中的凋亡基因表达
神经元MeCP2在K210和K249位点的乳酸化可改善卒中预后
为探究MeCP2乳酸化修饰在缺血性脑卒中中的作用,实验检测了MCAO小鼠缺血皮层中MeCP2 K210和K249位点乳酸化修饰水平。MCAO术后1天缺血皮层中MeCP2在K210和K249位点的乳酸化修饰水平显著升高,3天和7天逐渐下降,并接近基线水平。通过2-DG或4-CIN治疗均显著降低MeCP2在K210和K249位点的乳酸化修饰水平。这些发现表明,缺血性脑卒中后MeCP2在K210和K249位点的乳酸化修饰水平呈动态变化,在急性期迅速升高。2-DG和4-CIN对MeCP2乳酸化修饰的抑制作用表明,代谢改变可调控这种表观遗传修饰。
神经元特异性MeCP2条件性敲除(cKO)小鼠经腺相关病毒(AAV)回补野生型(WT)MeCP2可恢复K210/K249乳酸化,MCAO术后,观察到AAV-突变体组小鼠缺血皮层中促凋亡蛋白GVI PLA2和PDCD4的表达水平显著升高(图5D-F)。证实K210和K249位点的乳酸化修饰对于抑制卒中后这些凋亡标志物的表达至关重要,且是一种内在神经保护机制,其缺失会导致缺血性损伤加重和功能预后恶化。
为阐明MeCP2乳酸化修饰的调控机制,在Neuro-2a细胞中开展了一系列针对组蛋白去乙酰化酶(HDACs)和乙酰转移酶的敲低实验。曲古抑菌素A(TSA)治疗可显著增加MeCP2在K210和K249位点的乳酸化修饰水平。p300乙酰转移酶的敲低显著降低了MeCP2的乳酸化修饰水平。MeCP2、p300和HDAC3之间存在相互作用,揭示了涉及HDAC3和p300的复杂调控机制,参与MeCP2乳酸化修饰的调控。
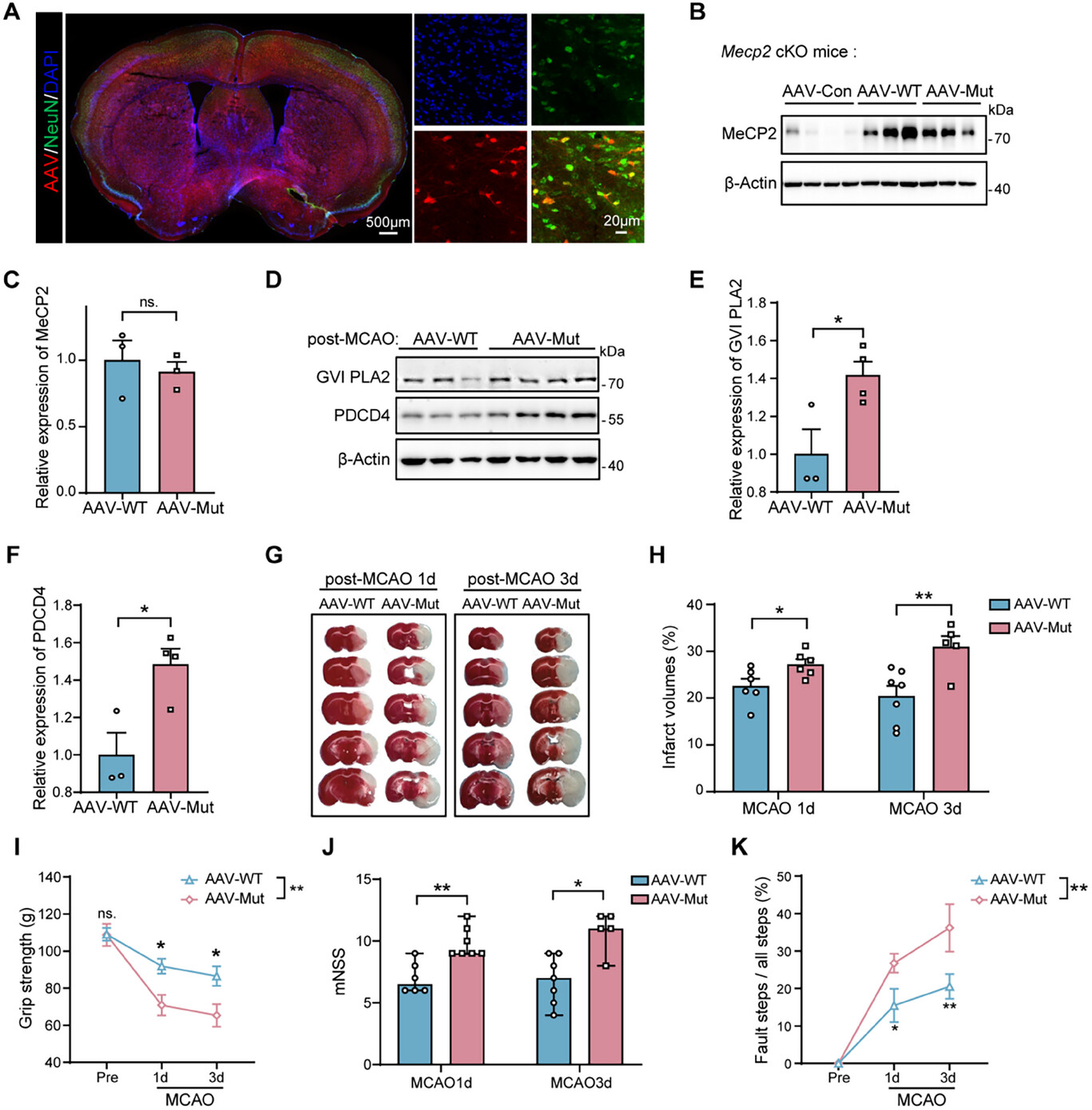
图5 神经元MeCP2蛋白在K210和K249位点的乳酸化可改善卒中预后
HDAC3与p300在缺血性脑卒中中调控MeCP2乳酸化
为探究HDAC3和p300对MeCP2乳酸化的调控作用及其对缺血性脑卒中的影响,作者在MCAO小鼠模型再灌注12小时后,分别使用选择性HDAC3抑制剂RGFP966或p300酶激活剂CTB进行治疗。显示RGFP966治疗可显著提高MeCP2在K210和K249位点的乳酸化水平,且显著减少了MCAO后1天和3天的脑梗死体积(图6A-D)。与此一致,经CTB治疗的卒中小鼠具有同样表现(图6H、I)。综上结果,抑制HDAC3或激活p300均可增强MeCP2的乳酸化修饰,进而减轻缺血性脑损伤并改善神经功能预后。
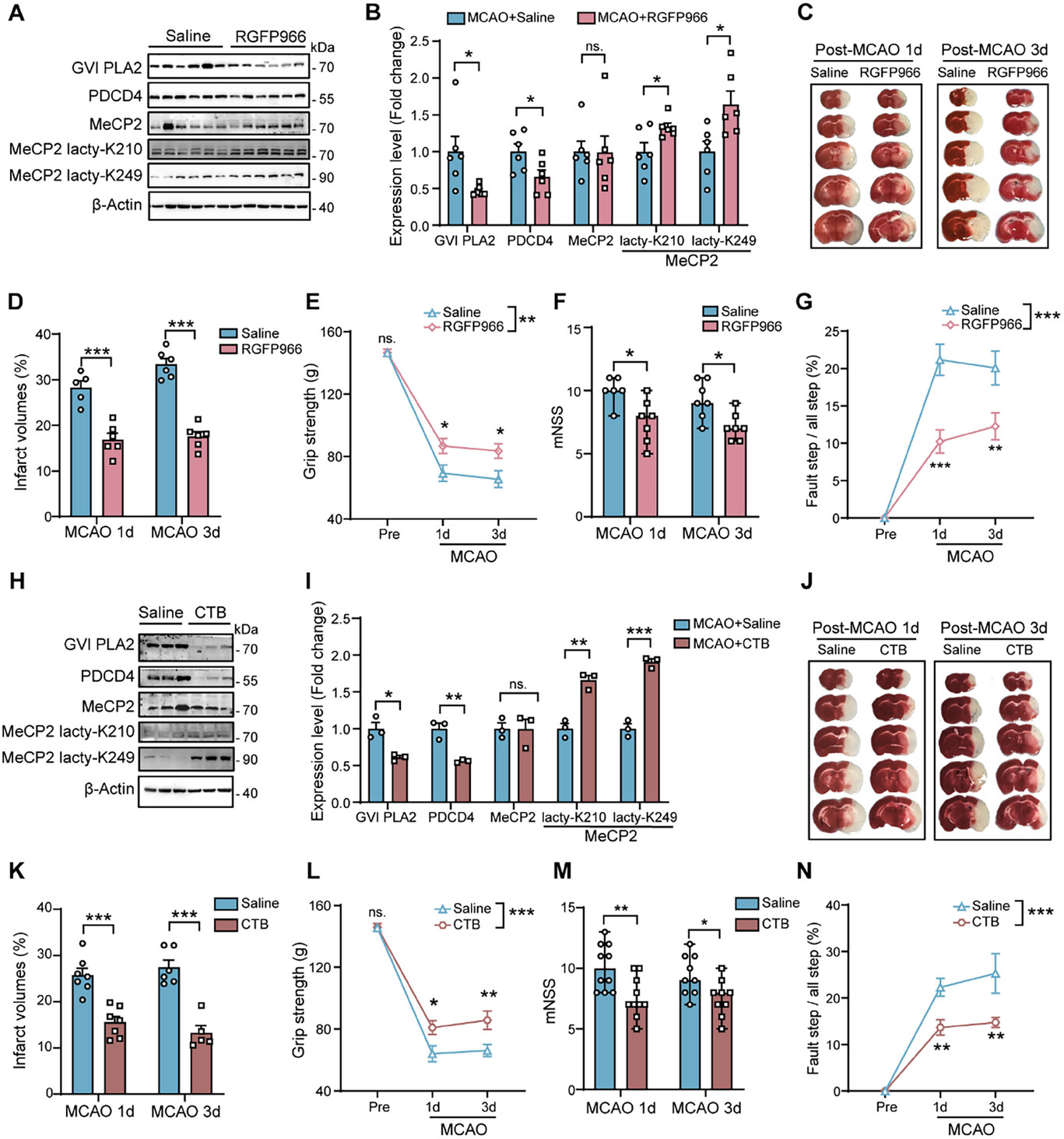
图6 HDAC3和p300在调节缺血性卒中中MeCP2的乳酸化过程中发挥作用
讨 论
本研究首次阐明非组蛋白MeCP2的乳酸化修饰在缺血性卒中中发挥关键神经保护作用:
(1)缺血诱导的乳酸积聚通过蛋白质乳酸化修饰而非单纯能量补充机制保护神经元;
(2)MeCP2-K210/K249乳酸化增强其对Pdcd4/Pla2g6启动子区甲基化CpG的结合,转录抑制促凋亡基因;
(3)HDAC3与p300分别作为去乳酸化酶与乳酸化酶,可动态调控MeCP2功能;
(4)药理激活MeCP2乳酸化(RGFP966、CTB、NALA)可显著改善小鼠卒中结局。
鉴于人类MeCP2-K210位点存在SNP,该位点的乳酸化缺陷可能影响卒中易感性与预后,值得临床进一步验证。通过靶向调控HDAC3和p300来干预MeCP2乳酸化,在缺血性脑卒中治疗中具有潜在的应用价值。
实验延展
基于活体实时监测的MeCP2乳酸化动态调控研究
既往研究发现,缺血性脑卒中后脑内乳酸积聚通过诱导MeCP2蛋白K210/K249位点乳酸化修饰,转录抑制促凋亡基因Pdcd4/Pla2g6,从而发挥神经保护作用。然而,传统终点法检测难以揭示乳酸动态与乳酸化修饰之间的实时量化关系。
本研究拟引入活体脑内化学物质实时分析系统,突破这一局限。通过将高灵敏度乳酸微电极植入MCAO模型小鼠缺血半暗带,可在无需处死动物、无需离体取材的前提下,实时、原位、连续监测乳酸浓度的动态变化,其时间分辨率可达毫秒级,从而完整捕捉 MCAO 模型中缺血 — 再灌注全周期的乳酸动态变化过程。

引入活体脑化学物质实时分析系统后,本研究将从“离散、断点”升级为“连续、实时、量化”的全新范式,不仅可精细刻画乳酸-蛋白质乳酸化修饰-神经元的动态因果链,还能显著减少动物用量、增强数据可靠性,为将来临床代谢干预与药效验证等奠定技术基础,把MeCP2乳酸化研究更有效推向临床精准治疗。
