
服务热线

大脑半球的功能偏侧化(Hemispheric lateralization)在语言、运动及空间认知等领域已得到充分研究。近年来,这一概念逐渐被拓展至中枢自主神经系统对外周器官的调控领域[1-4]。基于对肾脏、胸腺等对称器官的跨神经元追踪研究,提示存在“中枢对对称器官的对侧控制”现象[5-7]。然而,对于肝脏、心脏、胃等非对称器官,是否也存在类似的对侧调控机制,其解剖结构与功能之间的联系仍不清楚。
在代谢稳态方面,肝葡萄糖产生(Hepatic glucose production, HGP)是维持血糖平衡的关键环节之一,其中交感神经发挥重要调控作用[8]。尽管如此,交感神经如何实现对不同肝叶的精细调控,目前仍未得到系统阐明。
中国药科大学谢昊教授研究团队在eLife发表以“Symmetric brain-liver circuits mediate lateralized regulation of hepatic glucose output”为题的文章,围绕“脑-肝回路如何介导肝糖输出的精细肝叶调控”展开了系统研究。该研究以延髓LPGi脑区为切入点,综合运用伪狂犬病毒(PRV)跨突触追踪、化学遗传学与光遗传学等技术手段,揭示了以下发现:
1.LPGi向肝叶呈对称性投射,且表现出向对侧肝叶的支配优势;
2.交感神经调控的“对侧性”主要源于肝门区内交感神经纤维的交叉支配;
3.在单侧肝叶去神经后,存在由对侧LPGi触发的神经适应性代偿机制,以维持系统血糖稳态。

1. LPGi向不同肝叶的投射具有对侧优势性
研究人员首先确认了交感神经支配是所有肝叶的共同特征。组织透明化结合TH染色显示,尽管各肝叶体积不同,但交感神经纤维密度相似(图1A)。通过向各肝叶注射PRV进行多突触逆行追踪,发现LPGi神经元呈现明确的对侧投射模式:注射左外叶和中叶主要在右侧LPGi标记神经元,注射右后叶、右前叶和尾状叶则主要标记左侧LPGi(图1B, 1C)。这证实了LPGi的对称支配规律,即每个LPGi半球优先支配对侧肝叶(图1D)。为验证此模式,在右前叶和中叶分别注射PRV-EGFP和PRV-mRFP进行双标记。结果显示,左侧LPGi中73.7%的PRV⁺神经元投射至右前叶,右侧LPGi中62.5%投射至中叶(图1E, 1F)。部分神经元存在共标,提示除对侧优势支配外,少量LPGi神经元可能同时支配双侧肝叶。综上,研究明确了LPGi对肝叶的对侧优势投射模式(图1),为后续揭示“脑-肝”代谢调控环路的侧向化组织提供了解剖基础。
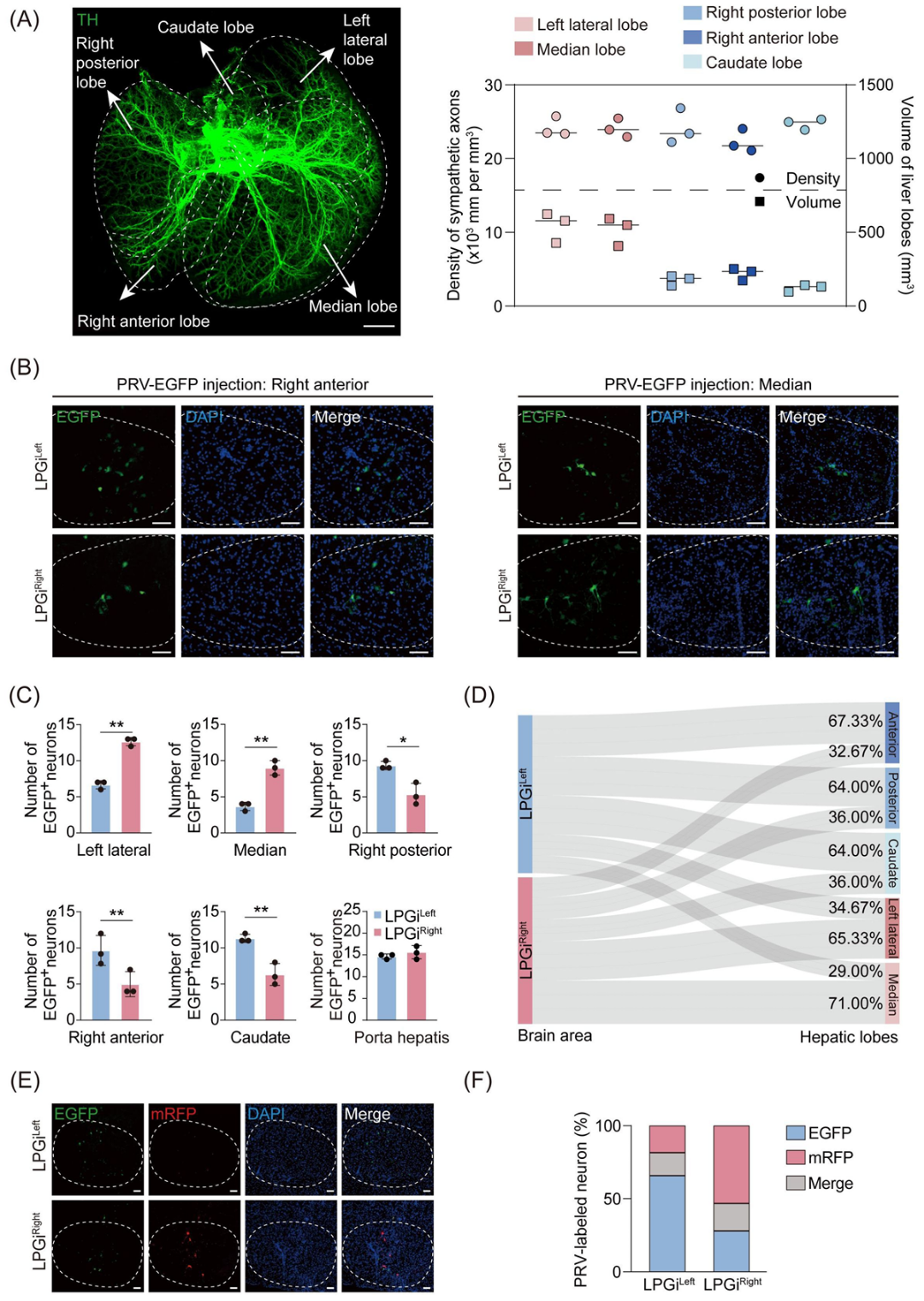
图1 大脑向对侧肝脏投射
2. LPGi侧向化激活对肝糖生成(HGP)的差异性调控
为探究该侧向化投射的功能意义,研究人员通过化学遗传学方法选择性激活LPGi GABA能神经元(图2A)。结果显示,激活左、右或双侧LPGi均显著升高血糖,其曲线下面积(AUC)分别增加27%、34%与52%,且右侧激活引起的血糖变化高于左侧(图2A)。分子水平上,激活一侧LPGi 1小时后,对侧肝叶中糖原磷酸化酶(pPYGL)与糖原合酶(pGS)的磷酸化水平显著上升:左侧激活主要升高右前叶pPYGL/pGS,右侧激活则对中叶作用更强(图2B-2D)。双侧激活可进一步协同提升两肝叶的磷酸化水平。
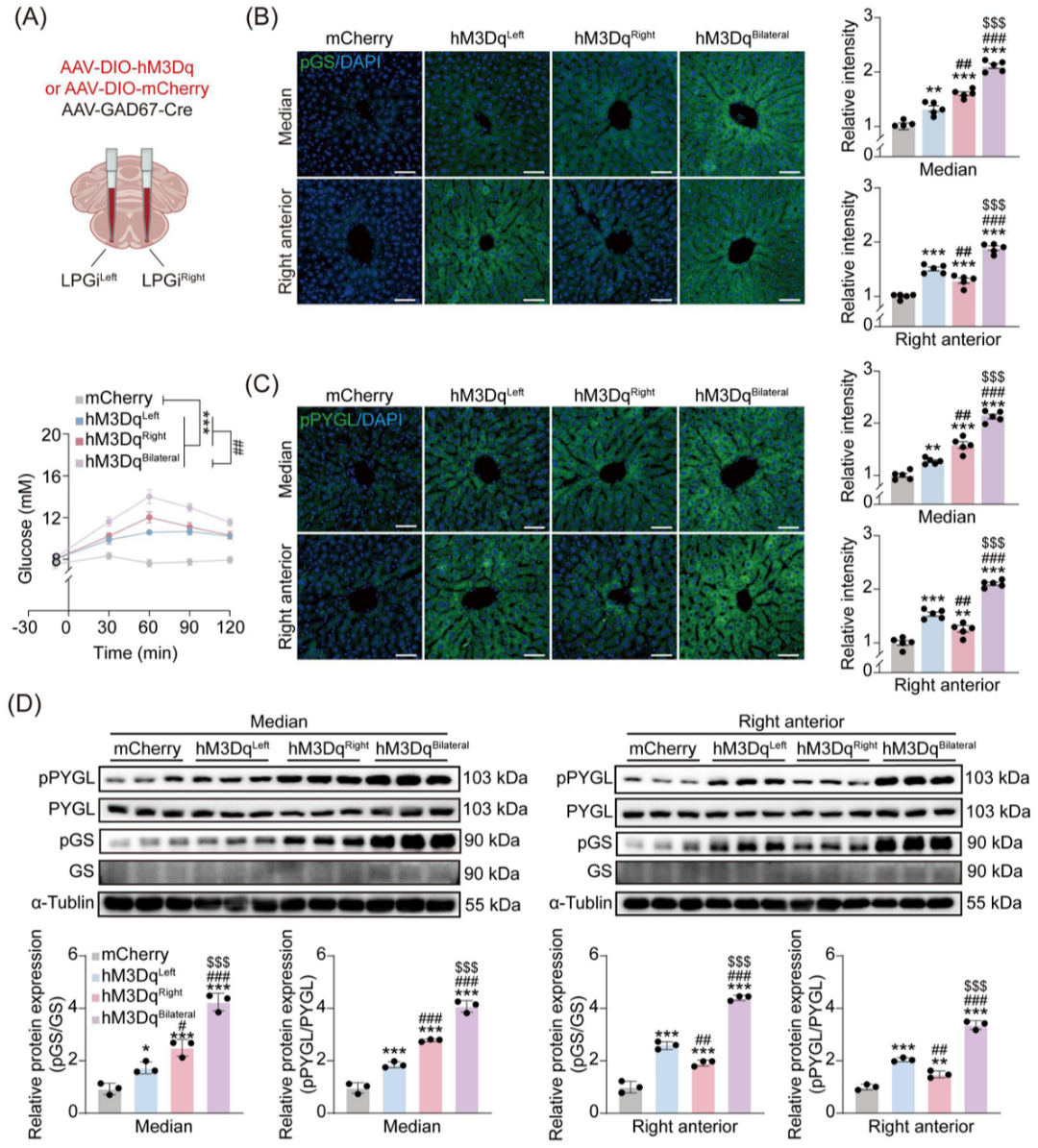
图2 LPGi 刺激通过促进对侧、特定叶区的肝糖原分解,从而升高血糖
3. 单侧肝去神经支配后的代偿性神经反应
尽管在对称性器官中,单侧损伤后的代偿适应机制已被充分描述,但在肝脏这类非对称性器官中是否存在类似机制仍不清楚。为了验证这一点,研究人员使用6-羟多巴胺(6-OHDA)化学性去除了右侧或左侧肝叶的交感神经支配。尽管去神经肝叶缺乏直接的交感输入,但与对照组相比,系统性血糖水平并未改变(图3A-3C),提示剩余完整的肝脏部分产生了功能性代偿。进一步分析显示,在非去神经的肝叶中,pPYGL和pGS的表达增加,肝内NE水平升高,且出现糖原消耗(图3D-3H)。为阐明其潜在机制,研究人员检测了单侧肝去神经后LPGi中c-FOS的表达。右侧肝叶去神经增加了左侧LPGi的c-FOS表达,反之亦然(图3I)。这表明,对侧LPGi增强了对同侧(即未受损侧)完整肝叶的交感神经输出,从而代偿了对侧去神经肝叶的功能丧失。
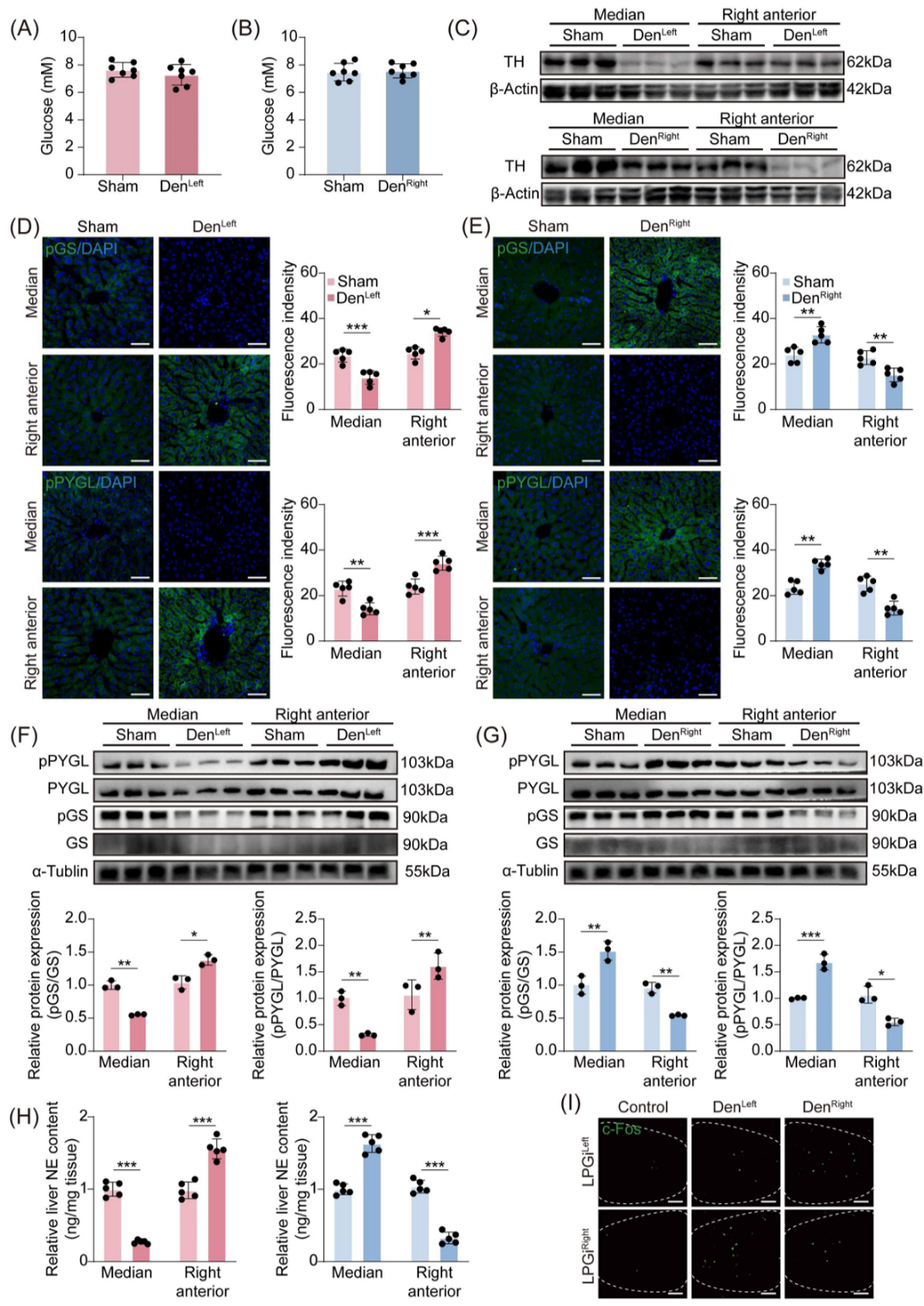
图3 LPGi 通过在对侧肝叶功能受损时补偿性地利用同侧肝叶来维持血糖平衡
4. 肝脏交感调控的周围侧交叉发生于肝门区
对侧神经环路通常源于中枢的交叉,例如在锥体交叉的皮质脊髓束用于控制肢体运动,以及在视交叉交叉的视觉通路用于半球对视野的处理。然而,大脑对肝脏的对侧调控发生在中枢还是外周是不确定。利用全鼠透明化技术,研究人员可视化了“脑-肝”交感神经环路,发现中枢投射直接自脑干沿交感链(SyC)下行至腹腔-上肠系膜神经节复合体(CG-SMG)(图4A)。而CG-SMG的交感神经束沿着肝门静脉深入肝脏(图4B)。研究人员推测这些神经束可能在肝门区域交叉后再延伸至各个肝叶。为验证此推测,研究人员通过向单侧CG注射AAV-TH-DIO-EGFP进行了单侧顺行追踪。结果显示了一种严格的对侧支配模式:左侧CG主要投射至右后叶、右前叶和尾状叶,而右侧CG则显著支配左外叶和中叶(图4C)。为了确认此模式,研究人员进行了双逆行追踪实验,将Alexa Fluor 647和555标记的麦胚凝集素(WGA)分别注射到左侧和右侧肝叶。结果与顺行追踪结果一致,证实了强烈的对侧支配(图4D)。为了确定这一支配模式是如何形成的,研究人员对出生后0至2周小鼠进行了组织透明化。研究人员发现,0.5天时交感神经束位于肝门部但尚未延伸入肝内(图4E,左);于1周时交感神经才开始向肝内生长(图4E,中);直到第2周,交感神经才完全伸入所有肝叶(图4E,右)。
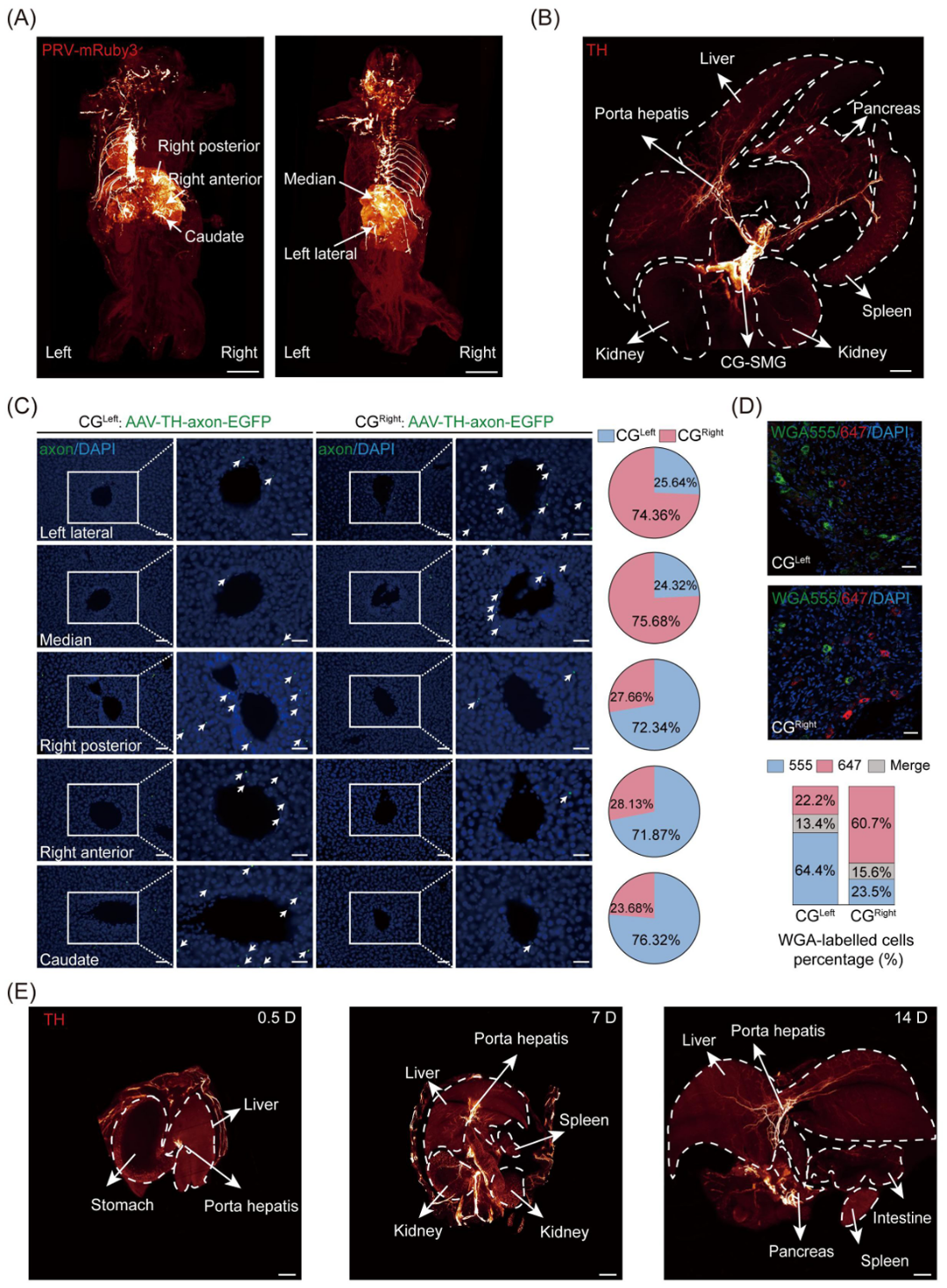
图4 通向肝脏的交感神经投射在肝门处交叉,这一结构在发育过程中逐渐形成
结论与讨论
延髓LPGi虽呈双侧对称分布,但对肝叶呈现明确的对侧优势支配。单侧LPGi激活可特异性增强对侧肝叶糖原分解与糖异生相关酶的活性,从而提升肝糖输出(HGP)并影响血糖水平。当单侧肝叶被去神经支配时,对侧LPGi能够通过增强它所支配的肝叶的神经递质释放,触发代偿性的代谢,形成一种维持血糖稳态的神经适应性机制。
最令人印象深刻的是,这种“对侧性”支配并非源于中枢神经纤维的交叉,而是在肝门区的交感神经纤维交叉,并实现了对对侧肝叶的调控。这一发现突破了以往认为中枢对侧调控的普遍模式,并将腹腔-上肠系膜神经节复合体(CG SMG)等外周神经节点确定为潜在的调控枢纽与干预靶点。
当然,本研究也提出若干有待深入探讨的问题:例如LPGi GABA能神经元的分子标识仍不明确;从小鼠模型到人类的应用转化仍需确定;此外,除葡萄糖代谢外,肝脏的脂质代谢、胆汁分泌等重要功能是否也遵循类似的偏侧调控规律尚需验证。
原文链接:https://doi.org/10.7554/eLife.109599.1
拓展阅读
以上研究揭示了延髓LPGi脑区通过交感神经对肝叶实施对侧支配的解剖与功能机制,为理解中枢自主神经系统调控外周葡萄糖代谢提供了新视角。然而,葡萄糖稳态的维持涉及多层次神经调控网络的协同作用,包括中枢感知、外周执行以及肠道-肝脏-大脑之间的信息整合。
郝海平、谢昊团队曾在Cell Metabolism期刊发表题为“Galnt2 neurons in the ventromedial hypothalamus counterregulate hypoglycemia via a brain-liver neurocircuit”的文章,揭示了一条由下丘脑腹内侧核Galnt2阳性神经元发起,经由脑-肝神经回路直接感知并对抗神经低血糖的全新机制。提出了血糖反调节的双相模型,为理解大脑在能量危机中的“终极防御”策略提供了新框架,为代谢性疾病的治疗开辟了新途径。
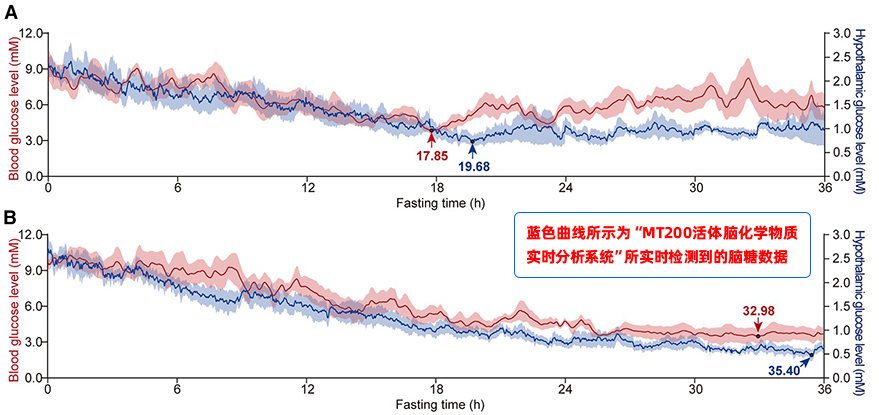
该研究应用了铭泰佳信自主研发的活体脑化学物质实时分析系统,对自由活动小鼠下丘脑腹内侧核区域的细胞外葡萄糖浓度进行了在体原位实时动态监测。该技术提供的高时间分辨率的在体脑糖数据,使其充当了“大脑血糖监测仪”的角色,与传统的机体血糖监测共同阐明脑-组织血糖调控规律,是连接全身血糖变化与中枢神经元活动的桥梁,为研究者提出“阈值依赖性脑糖感知”和“双相反调节模型”这一核心创新理论提供了直接实验依据,使整个研究逻辑链条更加完整。
研究亮点:
1、双相模型解释了低血糖的代偿反应。
2、VMH葡萄糖抑制神经元在神经低血糖感知方面功能至关重要。
3、脑-肝神经回路突显了低血糖的代偿反应。
4、Galnt2作为VMH葡萄糖抑制神经元的遗传标记和分子刹车。
研究发现并阐明了一条由下丘脑Galnt2阳性葡萄糖抑制性神经元介导、经VMH→PVH→LPGi→肝脏交感神经通路的全新“脑-肝”神经回路。该通路能够直接感知脑内葡萄糖水平下降,在血糖降至约4.0 mM(对应下丘脑葡萄糖约1.0 mM)的生理阈值时被激活,并通过增强肝内去甲肾上腺素释放及β2-肾上腺素能受体信号,快速驱动肝葡萄糖生成。研究进一步揭示Galnt2作为该通路的“分子刹车”,通过O-GalNAc糖基化修饰精细调控神经元的兴奋性阈值,防止其在正常生理状态下过度激活。
这项工作不仅首次完整描绘了大脑直接感知血糖危机并通过特异性神经通路指令肝脏产糖的完整机制,建立了“阈值依赖型双相血糖反调节”新模型,更革新了长期以来主要依赖激素调控血糖的传统认知。该发现为理解低血糖感知异常、糖尿病血糖波动等临床问题提供了全新理论框架,也为开发针对中枢神经通路的新型代谢疾病治疗策略奠定了重要基础。